-
随着核技术的飞速发展,从事辐射相关职业的人越来越多。由于遗传背景的差异,每个人对辐射的敏感性不同,有的人对辐射十分敏感,有的人则具有较强的抗性。遭受相同水平的辐射暴露,辐射抗性人群有可能不会出现任何症状,而辐射敏感人群则相对容易表现出辐射损伤,甚至需要采取医学救治。对辐射相对敏感的人如果在核电站、铀矿等辐射相对较强的环境长期工作,相对容易出现免疫力低下,甚至生病;对辐射相对抗性的人群可能更胜任辐射相关的职业。但由于各方面的原因,个体辐射敏感性的筛查并未受到重视,其检测标准也尚未建立。
以往研究发现,动物或病人接受辐照后早期出现外周血白细胞数急剧下降的现象,下降幅度与辐照剂量呈正相关 [ 1- 3] ,因而成为辐射损伤的早期生物标志物。外周血淋巴细胞微核率 [ 4- 6] 和染色体畸变率 [ 7- 9] 分析被当作是经典的辐射损伤检测技术。近年来,
$\gamma $ H2AX焦点作为检测辐射损伤的间接方法,快速而灵敏 [ 10- 12] 。另外,8-羟基鸟嘌呤 [ 13- 15] 、染色质桥 [ 16- 17] 、细胞周期阻滞 [ 18- 20] 等也被用于表征辐射损伤的程度。理论上,接受相同水平的电离辐射后,辐射敏感人群和抗性人群在这些反映辐射损伤程度的生物学终点方面存在差异,均有可能作为辐射敏感性的评价指标。其中,细胞松弛素B阻断微核分析法(Cytokinesis-block Micronucleus,CBMN)可以对辐射生产活动、医疗照射和事故暴露的体内辐射照射进行评估,同时也可以对个人的体外辐射敏感性进行评估 [ 21- 23] 。作为首次研究个体辐射敏感性差异,尝试引用最经典的CBMN法分析,以期建立个体辐射敏感性的筛分标准,绘制个体辐射敏感性的剂量效应曲线。 -
研究对象:50名男性志愿者;平均年龄19.7岁,年龄最小18岁、最大23岁;问卷调查显示,所有志愿者的个人健康均为良好,无放射接触史,无家族遗传病史。
样品采集与照射:空腹静脉采血,肝素钠抗凝管收集,每位志愿者的外周血等分到6个Eppendorf管。分装后立即进行照射处理。辐射为225 kV、2.99 mA的X射线(X-RAD,Precision X ray,North Branford,美国),剂量为0.0, 0.5, 1.0, 1.5, 2.0和2.5 Gy,剂量率1 Gy/min,室温下辐照。
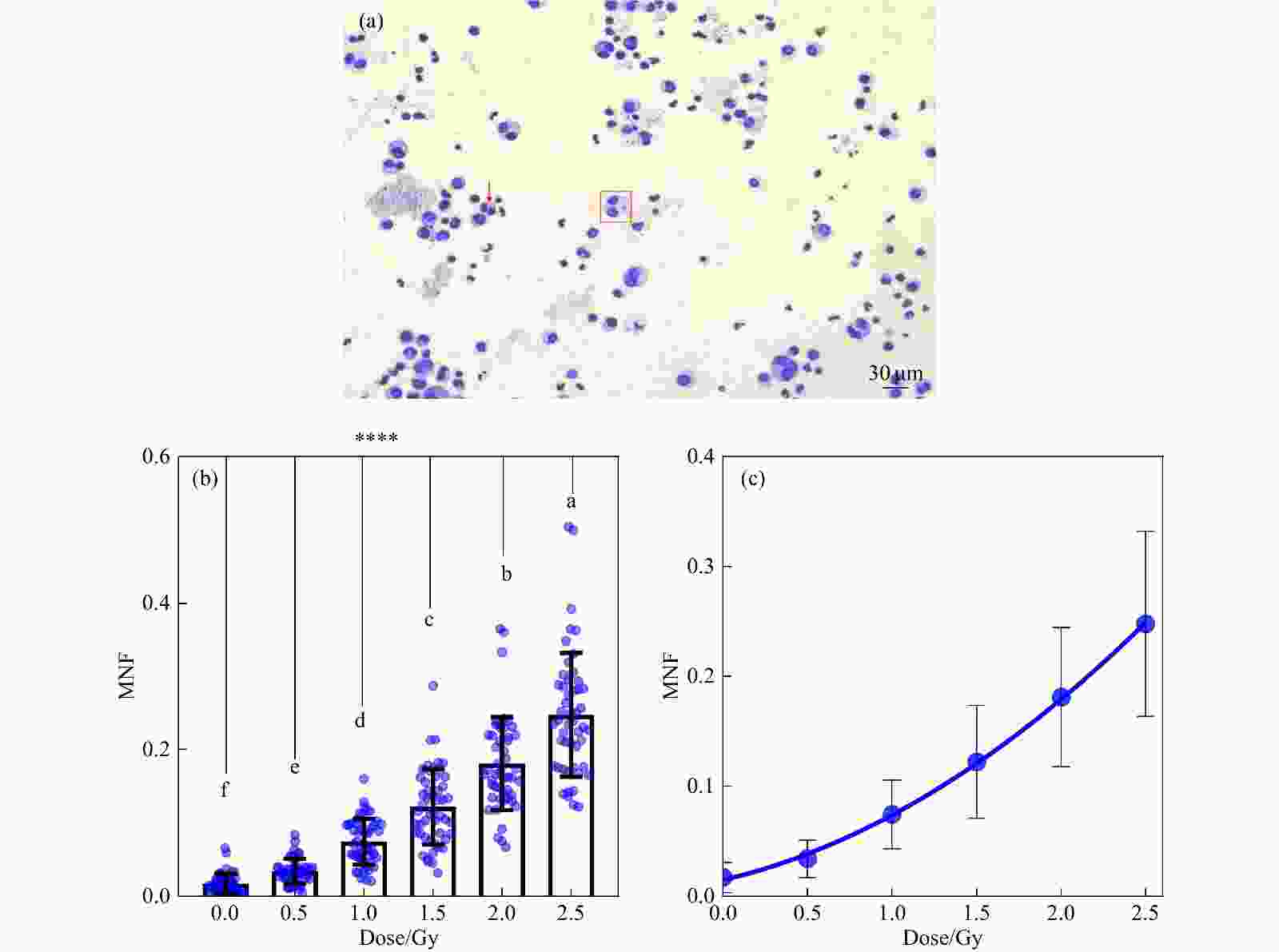
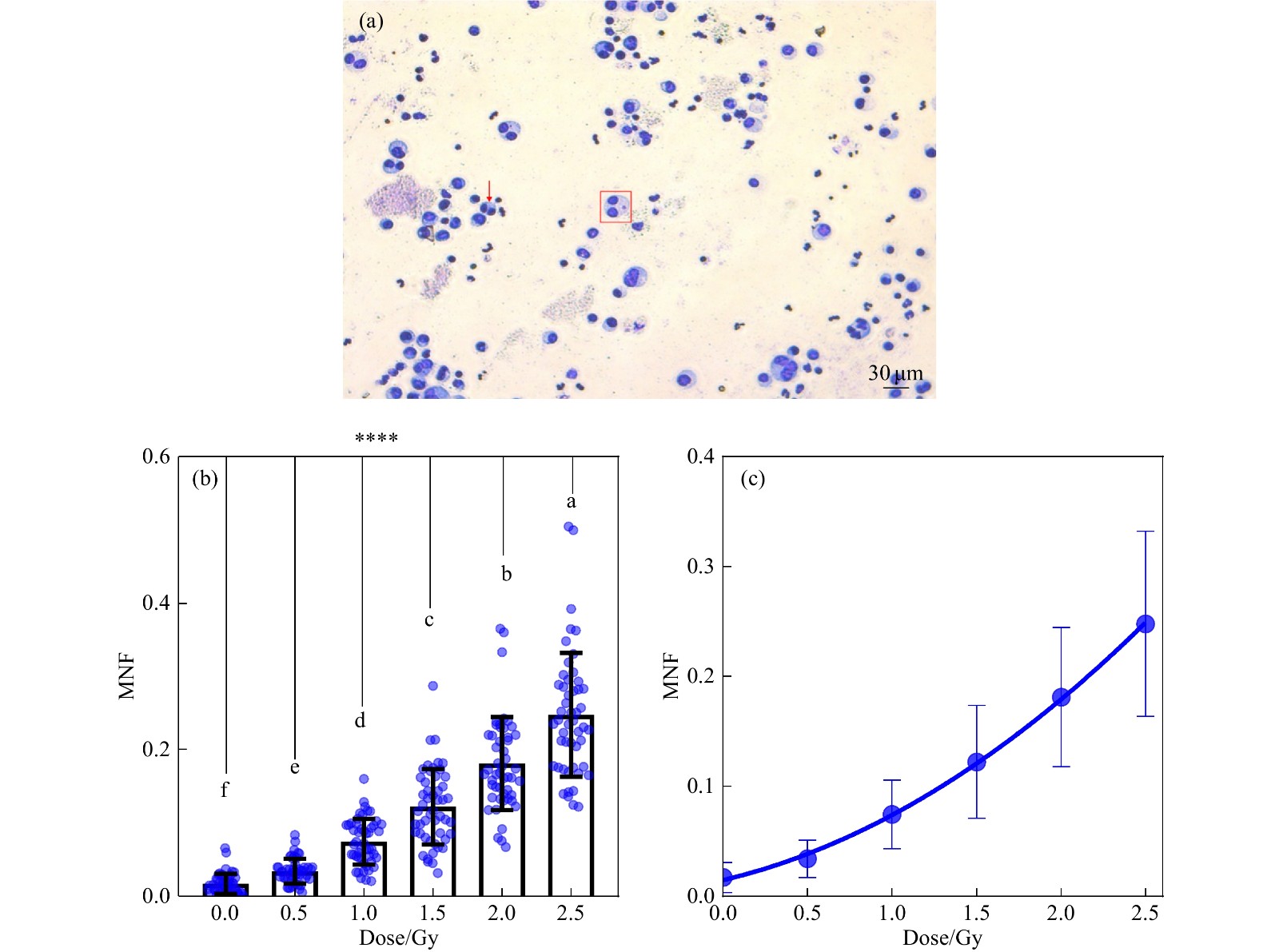
微核分析:辐照后,每个样品取500 μL,转移至5 mL外周血细胞培养液中,37 ℃恒温箱培养,44 h后加入细胞松弛素B(终浓度6 μg/mL),继续培养28 h后,2 000 r/min离心5 min,弃上清,在沉淀中加入8 mL、0.075 mol/L的KCl 溶液,于37℃低渗15 min,用2 mL固定液(甲醇:乙酸=3:1)终止低渗,1 500 r/min离心10 min,弃上清,用10 mL固定液重悬细胞,再次离心收集细胞,用固定液重悬后滴片;自然干燥后Giemsa染色,双盲法统计双核细胞数和带有微核的双核细胞数,每个样品至少统计500个双核细胞。微核率(Micronucleus Frequency,MNF) =带有微核的双核细胞数/双核细胞数×100% [ 图1(a)]。
统计方法:本文使用Shapiro-Wilk方法检验0.0, 0.5, 1.0, 1.5, 2.0和2.5 Gy辐射的各个组别原始数据分布类型。随后使用方差分析各个辐射点之间的MNF在各组之间的差异性,接着使用SNK(Student-Newman-Keuls)法计算具体有差异性的组别。以每个剂量点的平均MNF及其离散程度使用二阶多项拟合辐射诱导微核剂量效应选项中心方程曲线。本底MNF(自然环境中的辐射,包括人类和动物在体内和体外的宇宙射线及天然放射性元素发出射线辐照后,体内产生的染色体碎片)与辐射敏感性之间的相关性使用Spearman秩和相关计算。各个计量点本底MNF与辐射敏感性之间的相关性使用线性相关来实现。上述所有的统计方法使用的软件为SAS 9.4(北卡罗来纳州立大学)。
-
在数据分析之前,我们先用Shapiro-Wilk法对数据的分布类型进行分析。结果显示:0.0, 0.5, 1.0, 1.5, 2.0 和2.5 Gy辐射剂量点的原始数据均服从正态分布, P值分别是0.260, 0.072, 0.390, 0.100, 0.250和0.290,均大于0.050拒绝零假设( H 0),服从正态分布。随后使用方差分析得出 F=39.65; P<0.000 1,提示各组之间MNF有差异性,要深入研究具体组别之间的差异性,使用SNK法得出每两组之间均有显著差异性( P<0.000 1),并且随着辐照剂量的增加MNF也逐渐增加。此结果与文献报道一致 [ 24- 25] ,MNF诱导呈剂量依赖性,每一个样本的MNF都随着辐照剂量的增加而增加[ 图1(b)],剂量效应曲线均符合线性平方模型;但是,相同剂量辐照不同样本诱导的MNF存在差异[ 图1(b)],体现出个体辐射敏感性的差异。以50个样本的MNF平均值及其分散程度,拟合剂量效应二阶多项的中心方程为MNF=0.014 7+0.036 2D+0.023 1D 2 [ 图1(c),蓝色线条],回归系数 r为0.726。
-
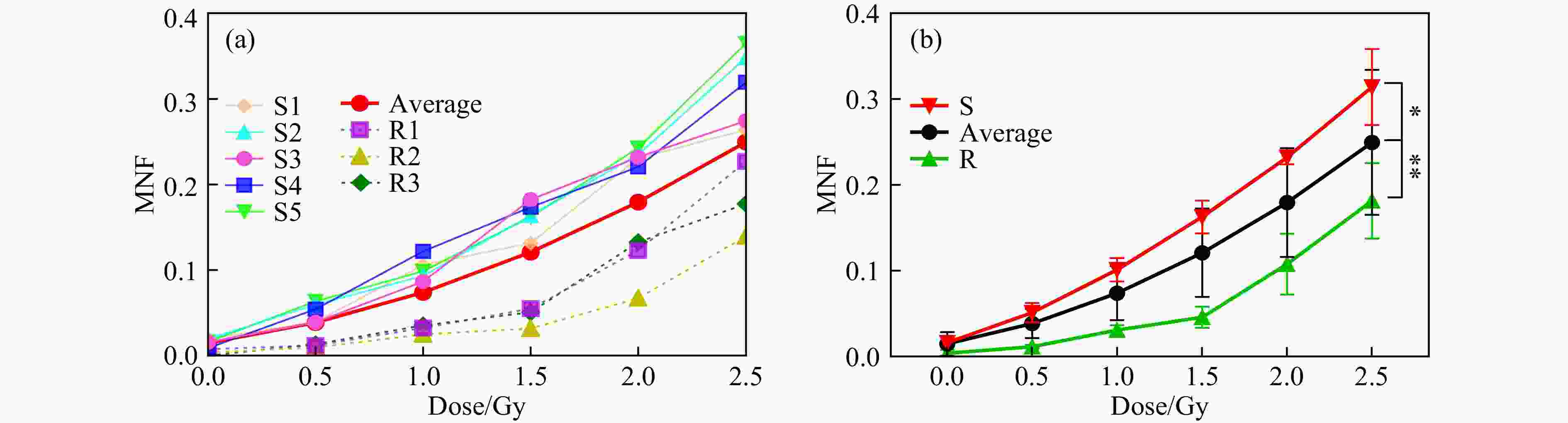
个体辐射敏感性的界定目前国内外都还没有标准。参照辐射损伤实验研究和临床肿瘤放射治疗的惯例,一般可以通过比较相同辐照剂量(例如2 Gy)诱导的生物效应的高低,或者达到相同的生物学终点需要的辐射剂量大小两种方法来区分敏感性,相同辐照剂量诱导的生物效应高的辐射敏感性高,或者达到相同的生物学终点需要的辐射剂量小的辐射敏感性高。两种方法均是采用单个剂量点来进行评价,往往需要通过足够的重复实验次数来获得可靠的实验结果。但是,考虑实际工作中反复抽取被试者的血液可操作性低,每个样本(即每位志愿者)MNF的测定很难进行三次以上的有效重复,为了降低单次实验的误差,我们测定了每个样本6个辐照剂量点的微核数据,据此绘制辐射诱导微核的剂量效应曲线,“以线代点”,以量效关系来确定个体辐射敏感性。然后,以50个样本每个剂量诱导的MNF平均值来绘制标准剂量效应曲线。最后,将每个样本的剂量效应曲线与标准剂量效应曲线进行比对,所有5个剂量点(不含本底)的MNF均高于平均值的样本,定义为辐射敏感人(群);每个样本所有5个剂量点的MNF均低于平均值的定义为辐射抗性人(群);5个剂量点中有的高于平均值、有的低于或者等于平均值的,定义为普通人(群),具体示例如 图2(a)所示;随后,敏感人群的MNF均值、抗性人群MNF均值分别与50位志愿者均值进行统计学分析[ 图2(b)],分析结果表明:在各个剂量点下,敏感人群、抗性人群均与50位志愿者之间存在MNF差别,具有统计学差异。依据此标准我们发现,50个样本中对辐射敏感的有13人(占26%)、对辐射抗性的14人(占28%),基本符合正态分布(见 表1)。
表 1 个体辐射敏感性的分布
背景微核率 合计人数 敏感人数 普通人数 抗性人数 敏感人群比例/% 普通人群比例/% 抗性人群比例/% 全部志愿者 50 13 23 14 26.0 46.0 28.0 高 13 6 6 1 46.2 46.2 7.6 中 22 6 11 5 27.3 50.0 22.7 低 15 1 6 8 6.7 40.0 53.3 -
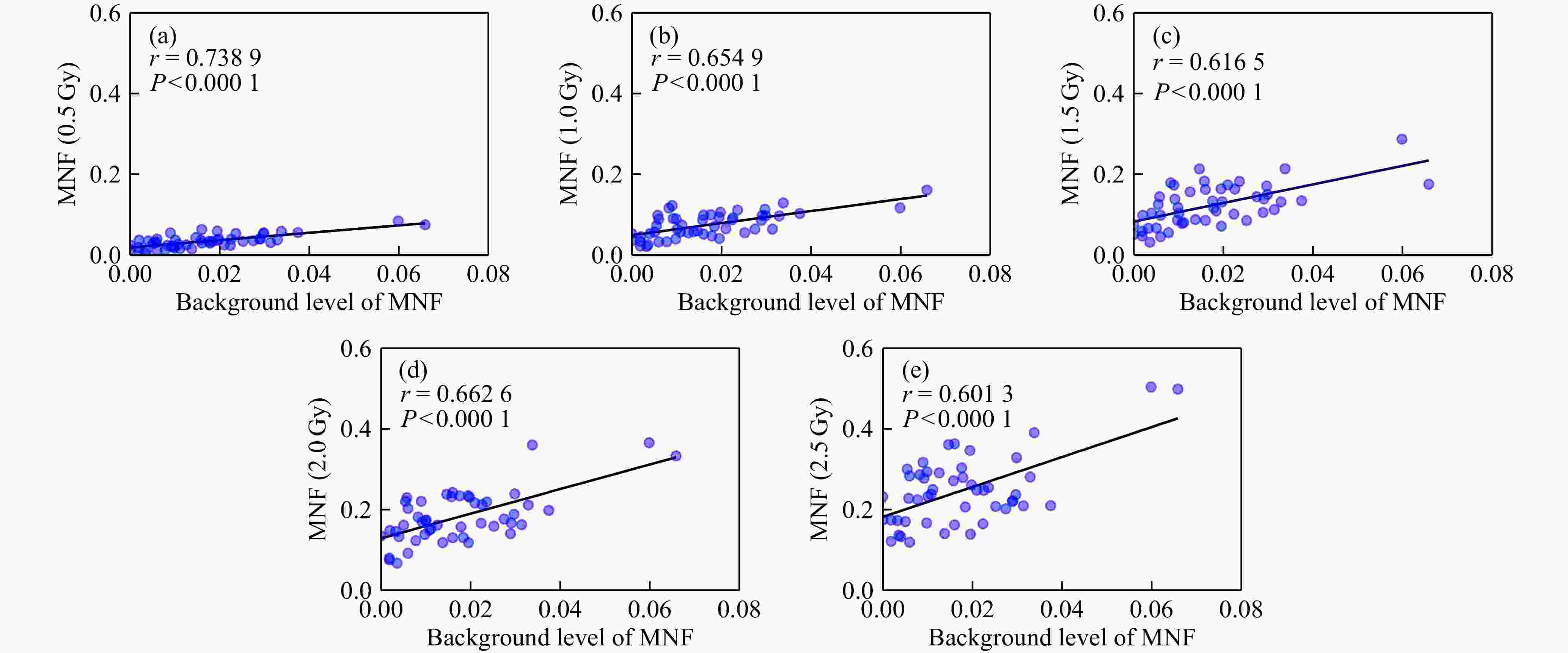
按照3.2节划分个体辐射敏感性的方法我们将人群分为辐射敏感人群、普通人群和抵抗人群( 表1)。15位低本底的志愿者中仅1人(6.7%)对辐射敏感,却有8人(53.3%)对辐射抗性;13位高本底的自愿者中6人(46.2%)对辐射敏感,仅1人(7.6%)对辐射抗性。因此,我们分析个体敏感程度与本底MNF之间的相关性,由于数据为等级变量,我们采用等级变量的秩和相关分析来验证两个变量之间的相关性。结果发现:本底MNF和辐射敏感性呈正相关,即本底MNF低的样本中辐射敏感性人数少、抗性人群多;本底MNF高的样本中辐射敏感人数多、抗性人群少( 表1)。为了研究本底MNF与不同辐射后各个辐射剂量点MNF之间的相关性,使用线性相关做散点图并且进行拟合,结果如 图3所示,0.5, 1.0, 1.5, 2.0 和2.5 Gy分别照射后的MNF与本底MNF之间均呈现正相关。在各个辐射剂量点的相关系数 r分别是0.738 9, 0.654 9, 0.616 5, 0.662 6和0.601 3,并且 P值均小于0.05,说明在每个辐射剂量点均呈现出本底MNF越高则辐射敏感性越高的趋势。
-
个体辐射敏感性存在差异,但是目前国际上还没有鉴定个体辐射敏感性的方法和标准。在科研和临床肿瘤放疗中,常用照射剂量为2 Gy时的细胞存活分数(Survival Fraction,SF2)来反映肿瘤细胞对辐射的敏感性,SF2高的细胞辐射抗性强,SF2低的细胞辐射敏感性高 [ 26- 28] 。微核率往往与存活率呈负相关 [ 29- 30] 。CBMN法是检测辐射损伤和细胞辐射敏感性的经典实验技术之一 [ 5] ,微核率与辐照剂量的相关性好,实验可重复性高,考虑到个体辐射敏感性检测的可靠性、便捷性和可操作性,本实验采用经典的CBMN法,建立了基于X射线辐照诱导外周血淋巴细胞微核剂量效应曲线的个体辐射敏感性检测方法。
本实验首次设立了“以线代点”个体辐射敏感性的鉴定标准,即所有5个辐照剂量诱导的MNF均高于平均值的为辐射敏感人(群)、5个剂量点诱导的MNF均低于平均值的为辐射抗性人(群);并且研究结果发现,本底MNF与辐射敏感性呈正相关,与辐射抗性呈负相关性。虽然还需要大样验证本实验的结果,但是,这一发现有可能有效降低鉴定个体辐射敏感性的工作量,大幅提高个体辐射敏感性检测的效率,增加大样本分析的可行性。另外,本实验发现该标准的建立是一次有益的尝试,但具有一定的主观性,还需要不同科研小组加大样本量对其可靠性进行验证;同时,也需要对比不同的检测技术、不断优化技术流程来实现大规模、快速检测的可行性。
需要注意的是,个体辐射敏感性是由遗传背景决定,受到生理状态的影响。年龄、性别等因素会对本底微核率以及辐射诱导微核率有影响 [ 4, 31] ,而饮食 [ 32- 34] 、作息时间(昼夜节律) [ 35- 37] 、情绪 [ 38- 39] 等因素都会影响机体的生理状态,导致个体对辐射敏感性发生变化。界定个体辐射敏感性建议对受试者的生理状态作必要的限定,例如取样前一周内保持正常的作息时间,不得服用药物 [ 40] 、饮酒 [ 41] 、吸烟 [ 42- 43] 、剧烈运动 [ 44- 45] 等,取样时间统一(早晨
$7 \thicksim 9$ 点空腹采血)等;否则,检测结果会出现偏差,影响分析结果的可靠性。
Preliminary Study on Male Individual Radiosensitivity by Cytochalasin-B Blocked Micronucleus Assay
-
摘要: 初步研究了男性个体辐射敏感性的鉴定方法及标准。采集50名男性志愿者的外周血,分别给予不同剂量X射线照射,采用细胞松弛素B阻断双核法测定微核率(MNF),通过二阶多项拟合法,绘制微核剂量效应选项中心标准曲线,将个人微核剂量效应曲线与标准曲线比对后判断个体辐射敏感性。
$0.0\sim2.5 $ Gy剂量范围内,剂量效应二阶多项拟合的中心方程为(MNF=0.014 7+0.036 2D+0.023 1D 2, r=0.726)。50名志愿者中,辐射敏感的有13人,辐射抗性的有14人,基本符合正态分布。Spearman秩和相关分析结果显示,MNF在各个辐射剂量点与辐射敏感性均存在正相关,与辐射抗性呈负相关,MNF随剂量增加而增加。本研究初步建立了“以线代点”男性个体辐射敏感性鉴定方法,并发现男性外周血淋巴细胞的本底微核率与个体辐射敏感性呈正相关。Abstract: Methods and criteria for the identification of male individual radiosensitivity are investigated. The peripheral blood of 50 male volunteers was irradiated with different doses of X-ray, the micronucleus frequency(MNF) was measured by cytokinesis-B block micronucleus assay, and the central standard curve of micronucleus dose effect was drawn by second-order multinomial fitting method so that the individual dose-response curve of micronucleus was compared with the standard curve to judge individual radiosensitivity. In the dose range of 0.0~2.5 Gy, the central equation of second-order polynomial fit for dose effect is (MNF=0.014 7+0.036 2D+0.023 1D 2, R=0.726). Among the 50 male volunteers, 13 were sensitive to radiation (26.0%) and 14 were resistant (28.0%), which basically fits the normal distribution. Spearman rank correlation analysis showed that the MNF increased with the dose and there was a positive correlation between the background MNF and the radiosensitivity of each dose, but negative correlation with the radioresistance. In conclusion, a "curve-instead-of-dose" male individual radiosensitivity identification method was established. Moreover, it was found that the background of micronuclei in peripheral blood lymphocytes was positively correlated with individual radiosensitivity.-
Key words:
- male individual radiosensitivity /
- ionizing radiation /
- micronucleus /
- dose effect
-
表 1 个体辐射敏感性的分布
背景微核率 合计人数 敏感人数 普通人数 抗性人数 敏感人群比例/% 普通人群比例/% 抗性人群比例/% 全部志愿者 50 13 23 14 26.0 46.0 28.0 高 13 6 6 1 46.2 46.2 7.6 中 22 6 11 5 27.3 50.0 22.7 低 15 1 6 8 6.7 40.0 53.3 -
[1] SANZARI J K, WAN X S, MUEHLMATT A, et al. Life Sci Space Res (Amst), 2015(4): 11. doi: 10.1016/j.lssr.2014.12.002 [2] SUNDARAMOORTHY P, WANG Q, ZHENG Z, et al. Stem Cell Res Ther, 2017, 8(1): 263. doi: 10.1186/s13287-017-0711-2 [3] TERRONES-CAMPOS C, LEDERGERBER B, VOGELIUS I R, et al. Int J Radiat Oncol Biol Phys, 2019, 105(4): 812. doi: 10.1016/j.ijrobp.2019.07.013 [4] GAJSKI G, GERIĆ M, OREŠČANIN V, et al. Ecotoxicol Environ Saf, 2018, 148: 561. doi: 10.1016/j.ecoenv.2017.11.003 [5] MISZCZYK J, RAWOJĆ K. Int J Radiat Biol, 2020, 96(4): 424. doi: 10.1080/09553002.2020.1704907 [6] SIAMA Z, ZOSANG-ZUALI M, VANLALRUATI A, et al. Int J Radiat Biol, 2019, 95(6): 697. doi: 10.1080/09553002.2019.1571255 [7] DUTTA S, YASHAVARDDHAN M H, SRIVASTAVA N N, et al. Food Chem Toxicol, 2016, 91: 141. doi: 10.1016/j.fct.2016.03.007 [8] HADA M, IKEDA H, RHONE J R, et al. International Journal of Molecular Sciences, 2018, 20(1): 43. doi: 10.3390/ijms20010043 [9] TELLO CAJIAO J J, CARANTE M P, BERNAL RODRIGUEZ M A, et al. DNA repair, 2018, 64: 45. doi: 10.1016/j.dnarep.2018.02.006 [10] MENECEUR S, LÖCK S, GUDZIOL V, et al. Radiother Oncol, 2019, 137: 24. doi: 10.1016/j.radonc.2019.04.009 [11] RASSAMEGEVANON T, LÖCK S, BAUMANN M, et al. Radiother Oncol, 2019, 139: 94. doi: 10.1016/j.radonc.2019.06.038 [12] SIDDIQUI M S, FRANÇOIS M, FENECH M F, et al. Mutat Res Rev Mutat Res, 2015, 766: 1. doi: 10.1016/j.mrrev.2015.07.001 [13] ALSHYKHLY O R, FLEMING A M, BURROWS C J. J Org Chem, 2015, 80(14): 6996. doi: 10.1021/acs.joc.5b00689 [14] CALKINS M J, VARTANIAN V, OWEN N, et al. DNA repair, 2016, 48: 43. doi: 10.1016/j.dnarep.2016.10.010 [15] ONA K, OH D H. Br J Dermatol, 2015, 173(3): 751. doi: 10.1111/bjd.13862 [16] SCHRÖDER-HEURICH B, WIELAND B, LAVIN M F, et al. FASEB J, 2014, 28(3): 1331. doi: 10.1096/fj.13-236984 [17] CHO M G, AHN J H, CHOI H S, et al. Free Radic Biol Med, 2017, 108: 129. doi: 10.1016/j.freeradbiomed.2017.03.025 [18] ANBUMANI S, MOHANKUMAR M N. Ecotoxicol Environ Saf, 2015, 113: 18. doi: 10.1016/j.ecoenv.2014.11.011 [19] GUDKOV A V, KOMAROVA E A. R J Clin Invest, 2010, 120(7): 2270. doi: 10.1172/JCI43794 [20] SOYSA R, LAMPERT S, YUEN S, et al. J Hepatol, 2019, 71(3): 553. doi: 10.1016/j.jhep.2019.04.015 [21] SU C, HASKINS A H, KATO T A. Methods Mol Biol, 2019, 1984: 23. doi: 10.1007/978-1-4939-9432-8_3 [22] M FENECH A A M. Mutat Res, 1985, 147(1-2): 29. doi: 10.1016/0165-1161(85)90015-9 [23] FENECH M, KNASMUELLER S, BOLOGNESI C, et al. Mutat Res, 2020, 786: 108342. doi: 10.1016/j.mrrev.2020.108342 [24] KOYAMA S, NARITA E, SHINOHARA N, et al. Int J Radiat Biol, 2016, 92(12): 790. doi: 10.1080/09553002.2016.1221544 [25] KOYAMA S, NARITA E, SHINOHARA N, et al. J Radiat Res, 2018, 59(5): 547. doi: 10.1093/jrr/rry051 [26] BENTZEN S M. Radiotherapy and Oncolo Gy, 1997, 43: 121. doi: 10.1016/s0167-8140(97)01899-9 [27] KAUR E, GODA J S, GHORAI A, et al. Cell Oncol (Dordr), 2019, 42(1): 107. doi: 10.1007/s13402-018-0411-7 [28] POULILIOU S E, LIALIARIS T S, DIMITRIOU T, et al. Int J Radiat Oncol Biol Phys, 2015, 92(3): 667. doi: 10.1016/j.ijrobp.2015.02.023 [29] ANDREASSI M G, BORGHINI A, PULIGNANI S, et al. Radiation research, 2016, 186(3): 245. doi: 10.1667/RR14266.1 [30] TIWARI M, DIXIT B, PARVEZ S, et al. Biomed Pharmacother, 2017, 88: 203. doi: 10.1016/j.biopha.2016.12.129 [31] CAI T J, LU X, TIAN X L, et al. Mutat Res Genet Toxicol Environ Mutagen, 2018, 832: 29. doi: 10.1016/j.mrgentox.2018.06.013 [32] SUGIYAMA H, MISUMI M, BRENNER A, et al. Int J Cancer, 2020, 146(3): 635. doi: 10.1002/ijc.32275 [33] YEN C A, CURRAN S P. Exp Gerontol, 2016, 86: 106-12. doi: 10.1016/j.exger.2016.02.012 [34] ZAORSKY N G, CHURILLA T M, RUTH K, et al. Am J Clin Nutr, 2016, 104(6): 1583. doi: 10.3945/ajcn.115.119958 [35] GRIFFIN F, MARIGNOL L. Int J Radiat Biol, 2018, 94(5): 472. doi: 10.1080/09553002.2018.1446227 [36] KANAKOGLOU D S, MICHALETTOU T-D, VASILEIOU C, et al. International Journal of Molecular Sciences, 2020, 21(6): 1938. doi: 10.3390/ijms21061938 [37] SEUNG Y H J K P G, ANTHONY B. Sci Transl Med, 2018, 10(470): 1643. doi: 10.1126/scitranslmed.aau1643 [38] WHOOLERY C W, WALKER A K, RICHARDSON D R, et al. Radiation Research, 2017, 188(5): 532. doi: 10.1667/RR14797.1 [39] PARIHAR V K, ALLEN B D, CARESSI C, et al. Sci Rep, 2016, 6: 34774. doi: 10.1038/srep34774 [40] KINOSHITA A, WANIBUCHI H, MORIMURA K, et al. Carcinogenesis, 2003, 24(8): 1389. doi: 10.1093/carcin/bgg079 [41] NAKAJIMA T, NINOMIYA Y, NENOI M. International Journal of Molecular Sciences, 2018, 19(12): 3855. doi: 10.3390/ijms19123855 [42] CANISTRO D, VIVARELLI F, CIRILLO S, et al. Sci Rep, 2017, 7(1): 2028. doi: 10.1038/s41598-017-02317-8 [43] IMAOKA T, ISHII N, KAWAGUCHI I, et al. Int J Radiat Biol, 2016, 92(6): 289. doi: 10.3109/09553002.2016.1152413 [44] MORENO-VILLANUEVA M, KRAMER A, HAMMES T, et al. International Journal of Molecular Sciences, 2019, 20(12). doi: 10.3390/ijms20122999 [45] TRYFIDOU D V, MCCLEAN C, NIKOLAIDIS M G, et al. Sports Med, 2020, 50(1): 129. doi: 10.1007/s40279-019-01197-4 -





 下载:
下载:



 甘公网安备 62010202000723号
甘公网安备 62010202000723号